在肿瘤领域中,传统化疗新药Ⅰ期临床试验主要研究目的为进行剂量探索寻找最大耐受剂量(maximum tolerated dose, MTD)或II期推荐剂量(Recommended Phase 2 Dose, RP2D),并且要求需要降低分配受试者不合适剂量的概率。进入Ⅱ期临床试验,主要研究目的为确定有效性最高的剂量、探索新药的初步疗效和安全性,为Ⅲ期试验设计提供依据。此时,在进行剂量探索设计往往假设毒性和疗效均随着剂量的增长单调递增,但对于免疫和靶向治疗领域或ADC药物(Antibody-drug conjugates),剂量的提升并不代表疗效的增加,甚至还可能伴随疗效的降低。因此,采用MTD作为RP2D往往会导致差错,要最优化免疫及靶向治疗治疗利益,需同时关注毒性和疗效,识别最优生物学剂量optimal biological dose (OBD),即风险利益平衡点的剂量(risk-benefit trade-off)。
采用Phase Ⅰ/Ⅱ设计可以同时考虑毒性和疗效,识别最优RP2D,同时在一个试验设计中完成I期和Ⅱ期试验。因同时考虑毒性和疗效,需要一个模型同时拟合毒性和疗效结局,如Efftox设计和Lo-efftox设计(考虑延迟疗效)基于收集的疗效和毒性数据评估每个剂量对应的疗效和毒性联合的满意度(desirability),选择满意度最高的最为最优剂量[1]。Yanhong Zhou, J. Jack Lee and Ying Yuan 提出一个基于效用的贝叶斯最优区间(Utility-based Bayesian optimal interval, U-BOIN)Ⅰ/Ⅱ期设计以寻找OBD[2]。
01基本思想
U-BOIN设计
U-BOIN设计主要由无缝衔接的两阶段组成:
1. 使用贝叶斯最优区间(Bayesian optimal interval, BOIN)设计进行剂量爬坡,寻找安全性可接受的剂量范围,并且同时收集疗效数据;
2. 进入第二阶段,在可接受的剂量范围内,每个cohort结束后,基于第一阶段和第二阶段已收集的数据,更新每个剂量对应的后验效用估计,并通过此估计进行下一cohort的剂量分配选择(自适应决策),直至达到最大的预定样本量,选择效用最高的作为OBD。
U-BOIN使用效用(utility)的概念来评价疗效和毒性结局,效用定义为在某个剂量水平下发生某个疗效-毒性结局的分数,分数越高,代表该结局越好。
02优 势
U-BOIN设计
相较于其他Phase Ⅰ/Ⅱ 设计,U-BOIN具有以下优势:
易于操作执行(在试验设计时事先设置决策规则获得决策表,试验开始后研究者根据决策表分配剂量)
U-BOIN为模型辅助设计,没有复杂模型设计
对不同剂量的毒性和疗效独立建模,不假定任何参数结构,具有稳健、精确度高的特点
使用效用测量各剂量下疗效-毒性结局的desirability,操作更灵活
03U-BOIN设计具体流程
具体的流程图如下所示:
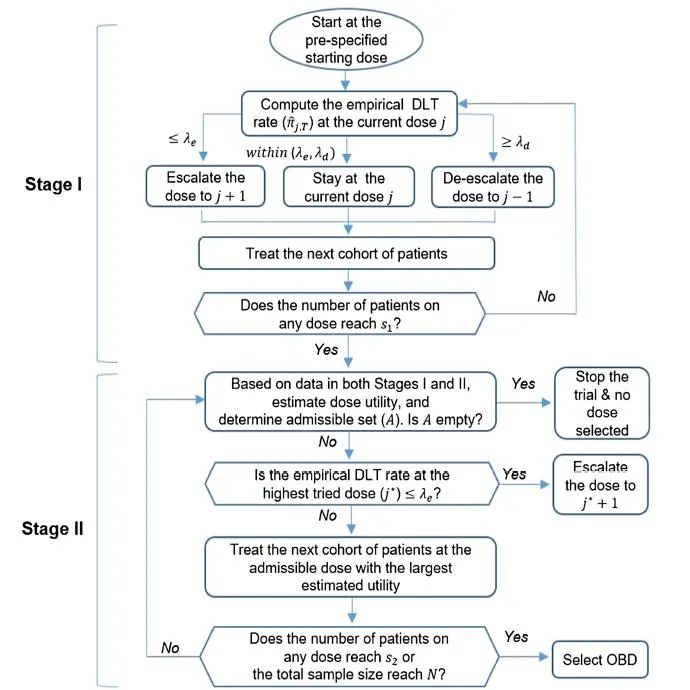
图源:参考文献[2]
第一阶段:
基于毒性结局数据,使用BOIN设计进行剂量爬坡,同时收集疗效数据,为第二阶段确定安全且有效的可接受剂量集。

第二阶段:

04软件应用
目前可通过袁鹰教授及言方荣教授团队开发的网站进行疗U-BOIN设计:http://trialdesign.cn/
具体的操作步骤如下:
1.首先,需要填写设置的剂量数、开始的剂量水平、队列大小、数目和评判第一阶段、第二阶段完成每个剂量下达到的患者数目(通常设S1=9~15,S2=18~24);
假设欲在恶性实体瘤患者中进行一项Phase I/II设计探索某试验药物的OBD:
剂量水平:5个
毒性结局:DLT发生率(toxicity with CTCAE grade 3 or higher)
疗效结局:二分类结局(肿瘤应答-完全缓解CR/部分缓解PR,稳定疾病状态SD/疾病进展PD)
剂量爬坡:样本量为54,设置18个队列,每个队列样本量设置为3,剂量爬坡从最低剂量开始试验
根据以上信息,我们在”Dose & Sample Size”中填写相应的信息,如下图所示:
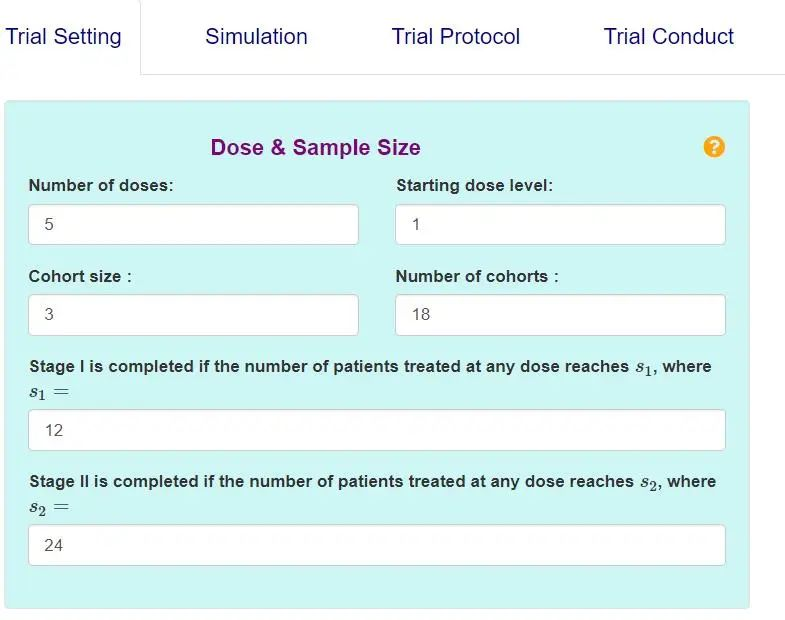
2.设置毒性和疗效结局的水平,目前可设置2水平或3水平;设置完毕后,填写每个疗效-毒性结局水平下的效用值;
根据1中假设例子的研究设计,毒性结局设置为两水平(是否发生CTCAE等级>=3以上的AE),疗效结局设置为两水平。
对于疗效-毒性复合结局,默认最好的结局(疗效应答,无DLT发生)效用值为100,最差的结局(疗效无应答,发生DLT)效用值为0,经临床医学和统计等多方判断当出现疗效无应答但无发生DLT的情况并不理想,赋予其效用值30,当出现疗效应答但发生DLT的情况尚可接受,赋予其效用值50。

3.设置最大可忍受的毒性率(如设置为0.3)和最小可接受的疗效应答率(如设置为0.2),并设置判定为可接受剂量的毒性和疗效应答概率界值(通常设置为0.95和0.9);

4.按下“Get Flow Chart and Decision Table”键,网页上出现U-BOIN的流程图和决策表,决策表分为第一阶段和第二阶段决策表:
第一阶段决策表输出已治疗的受试者人数下对应升剂量、降剂量和终止试验决策的DLT发生人数。
决策表具体使用:假设在第一阶段试验进行中,队列1中采用剂量水平1治疗的人数为3例,队列结束时需要采用决策表进行剂量爬坡决策,实际数据中3例中无受试者发生DLT结局,则按照决策表为下一队列受试者进行升剂量的决策。
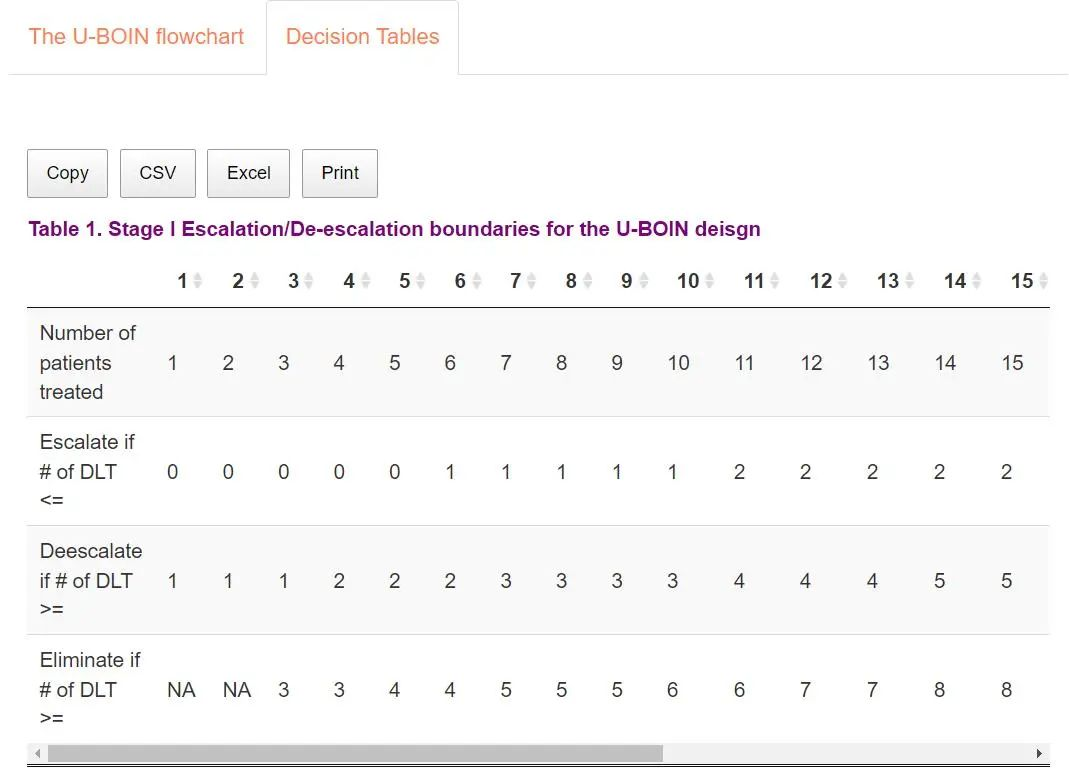
第二阶段决策表输出当已治疗的人数为3、6、9、12、15、18、21和24(先前设置S2为24)时各疗效结局水平的效用值大小,根据实际试验中不同决策时间点发生的结局情况按决策表获得每个剂量下对应的效用值。
决策表具体使用:假设在第二阶段试验进行中,已采用剂量水平1-3分别治疗3例、6例、15例受试者,在队列结束时需要进行剂量爬坡决策,根据每个剂量水平下实际发生的DLT发生人数和疗效应答人数在第二阶段决策表中找到对应的效用值,选择效用最高的作为下一队列的分配剂量。
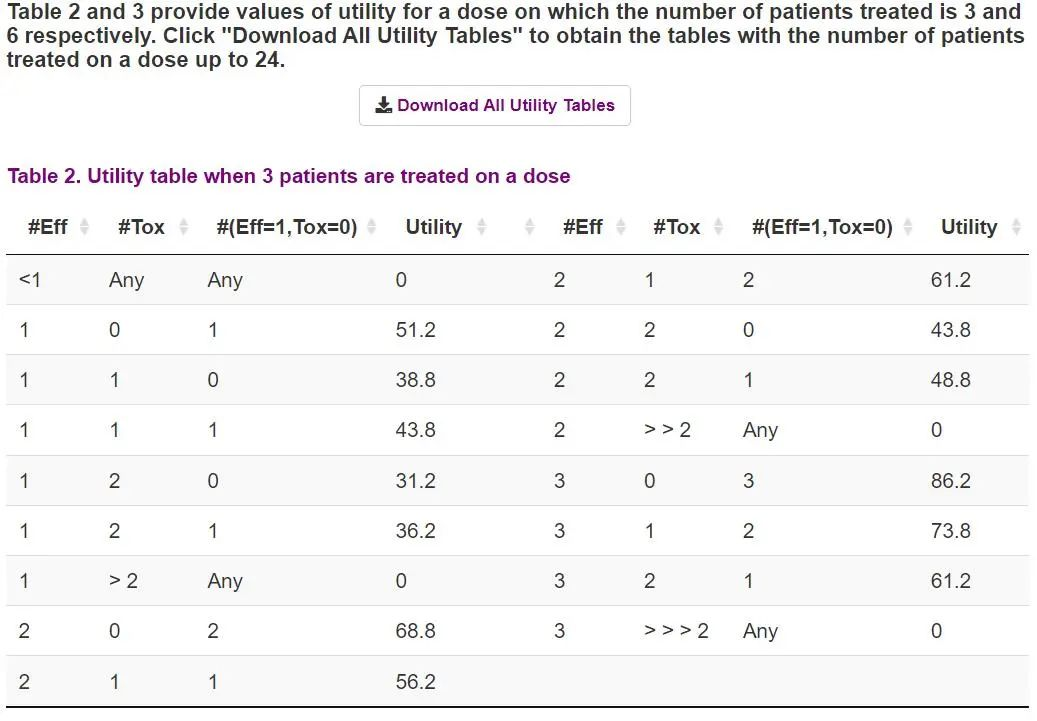
以上即是U-BOIN的学习内容,更多详细的设计理论小伙伴们可以移步参考文献继续学习~
参考文献
[1] Yan F, Thall PF, Lu KH, Gilbert MR, Yuan Y. Phase I-II clinical trial design: a state-of-the-art paradigm for dose finding. Ann Oncol. 2018 Mar 1;29(3):694-699. doi: 10.1093/annonc/mdx795.
[2] Zhou Y, Lee JJ, Yuan Y. A utility-based Bayesian optimal interval (U-BOIN) phase I/II design to identify the optimal biological dose for targeted and immune therapies. Stat Med. 2019 Dec 10;38(28):5299-5316. doi: 10.1002/sim.8361.