美国作为世界主要的药品生产和销售市场,是国内众多原辅包企业进入国际市场的首选。因此,了解美国DMF注册管理制度尤为重要。笔者基于自身成功申报美国DMF的经验,将从以下几方面言简意赅的介绍美国DMF注册管理制度,以期给业内同仁带来启发和帮助。
1. DMF简介

2. DMF申报流程
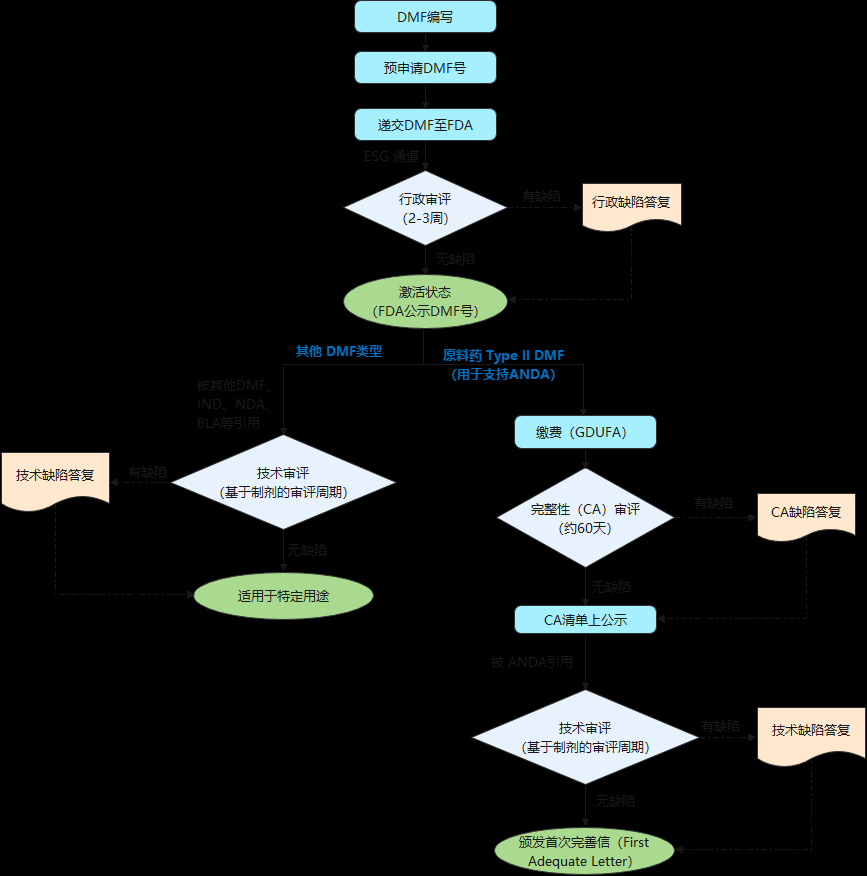
DMF申报流程解析 | |
A. 资料格式 | - 应按ICH M4的CTD格式整理申报资料,并以eCTD格式递交(Type III除外); - DMF的CTD各模块的主要内容见下表1; - DMF申报资料应为英文版本,任何非英文的部分均应进行翻译。 |
B. 资料递交 | - DMF递交时必须有DMF号; - 如果资料小于10G,必须通过ESG通道递交;如果资料超过10G,可以通过ESG通道或者物理媒介(如:CD-ROM)递交; - 在通过ESG提交时,从选项菜单中选择适当的中心(CDER 或 CBER)非常重要。若DMF持有人希望提交的资料在多个中心进行审评,则应咨询相应的各中心。 |
C. FDA审评 | - 行政审评:一般递交后2-3周内完成; - 完整性(CA)审评:对于原料药Type II DMF需按GDUFA进行缴费;缴费后方能进行CA审评,一般需要60天左右; - 技术审评:按DMF被IND、NDA、ANDA、BLA等关联引用时,才会进行技术审评。 |
D.FDA审评结果 | - DMF不存在批准或者不批准的说法; - 对于原料药Type II DMF,通过技术审评后,FDA会颁发First Adequate Letter或No Further Comment Letter。 |
表1:DMF申报资料内容简介 | |
模块1 | - Cover letter; - 行政信息(包括:DMF持有人、联系人/US代理人(若有)、生产商、Debarment声明); - 参考信息(授权信(LOA),授权人清单等) 其他信函(环境评估等。) |
模块2 | 总结模块3的内容(FDA强烈建议参考QbR指南) |
模块3 | 参考指南ICH guidance for industry M4Q: The CTD—Quality |
模块4 | - 适用于包含非临床评估的DMF: - 用于支持Type IV DMF 模块3 CMC中辅料安全性的非临床评估; - 用于支持Type II DMF 模块3 CMC中杂质安全性的非临床评估。 |
模块5 | 临床信息,如:Type IV DMF中的临床信息。 |
3. DMF增补 (Amendment)
4. DMF年报 (Annual report )
- 一般情况下,自DMF递交之日开始,每年需向FDA递交年报;
5. DMF关闭
- FDA关闭:若DMF未递交年报,FDA将关闭此DMF,并通知持有人或者代理。
- DMF持有人主动关闭:可以递交一个行政增补要求关闭DMF,同时递交一个已通知所有授权人DMF关闭的声明。
免责声明:本文系转载分享,文章观点、内容、图片及版权归原作者所有,如涉及侵权请联系删除!